Để sử dụng toàn bộ tiện ích nâng cao của Hệ Thống Pháp Luật vui lòng lựa chọn và đăng ký gói cước.
| BỘ Y TẾ | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
| Số: 369/QĐ-YDCT | Hà Nội, ngày 29 tháng 12 năm 2022 |
VỀ VIỆC CÔNG BỐ HỆ THỐNG QUẢN LÝ CHẤT LƯỢNG PHÙ HỢP TIÊU CHUẨN QUỐC GIA TCVN ISO 9001:2015
CỤC TRƯỞNG CỤC QUẢN LÝ Y, DƯỢC CỔ TRUYỀN
Căn cứ Quyết định số 19/2014/QĐ-TTg ngày 05/03/2014 của Thủ tướng Chính phủ về việc áp dụng Hệ thống quản lý Chất lượng theo Tiêu chuẩn quốc gia TCVN ISO 9001:2008 vào hoạt động của các cơ quan, tổ chức thuộc hệ thống hành chính Nhà nước;
Căn cứ Quyết định số 7666/QĐ-BYT ngày 25 tháng 12 năm 2018 của Bộ trưởng Bộ Y tế quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Cục Quản lý Y, Dược cổ truyền thuộc Bộ Y tế;
Căn cứ công văn số 419/BKHCN-TĐC ngày 21/02/2018 của Bộ Khoa học và Công nghệ hướng dẫn lộ trình việc xây dựng, áp dụng hệ thống quản lý chất lượng theo tiêu chuẩn quốc gia TCVN 9001:2015 vào hoạt động của cơ quan, tổ chức thuộc hệ thống hành chính nhà nước;
Theo đề nghị của Chánh Văn phòng Cục Quản lý Y, Dược cổ truyền,
Điều 1. Công bố Hệ thống quản lý chất lượng tại Cục Quản lý Y, Dược cổ truyền phù hợp với Tiêu chuẩn quốc gia TCVN ISO 9001:2015 đối với 01 quy trình xử lý công việc theo Phụ lục ban hành kèm theo Quyết định này.
Điều 2. Quyết định này có hiệu lực kể từ ngày ký ban hành.
Điều 3. Các ông, bà: Chánh Văn phòng Cục, Trưởng phòng Quản lý Dược cổ truyền và các bộ phận liên quan chịu trách nhiệm thi hành Quyết định này./.
|
| CỤC TRƯỞNG |
BẢN CÔNG BỐ HỆ THỐNG QUẢN LÝ CHẤT LƯỢNG TẠI CỤC QUẢN LÝ Y, DƯỢC CỔ TRUYỀN PHÙ HỢP TIÊU CHUẨN QUỐC GIA TCVN 9001:2015
(Ban hành kèm theo Quyết định số: 369/QĐ-YDCT ngày 29 tháng 12 năm 2022 của Cục trưởng Cục Quản lý Y, Dược cổ truyền - Bộ Y tế)
Cục Quản lý Y, Dược cổ truyền công bố Hệ thống quản lý Chất lượng tại Cục Quản lý Y, Dược cổ truyền phù hợp với Tiêu chuẩn quốc gia TCVN ISO 9001:2015 với 01 quy trình như sau:
I. Quy trình cấp công bố tiêu chuẩn chất lượng dược liệu.
Bản công bố này có hiệu lực kể từ ngày ban hành.
|
| Hà Nội, ngày 29 tháng 12 năm 2022 |
| CỤC QUẢN LÝ Y, DƯỢC CỔ TRUYỀN | |||
|
QUY TRÌNH QT.03.2022.QLD
| |||
|
| Người viết | Người kiểm tra | Người phê duyệt |
| Họ và tên | Nguyễn Văn Thắng | Phạm Văn Hải | Nguyễn Thế Thịnh |
| Chức vụ | Chuyên viên | PTP Quản lý DCT | Cục trưởng |
| Ký tên |
|
|
|
| Cục Quản lý YDCT | QT.03.2022.QLD |
| CỤC QUẢN LÝ | QUY TRÌNH | Mã số: QT.03.2022.QLD Ngày ban hành: Lần ban hành: 01 Tổng số trang: 05 |
NƠI NHẬN (ghi rõ nơi nhận rồi đánh dấu X ô bên cạnh)
THEO DÕI TÌNH TRẠNG SỬA ĐỔI (tình trạng sửa đổi so với bản trước đó)
|
Quy trình này nhằm quy chuẩn hóa quá trình công bố tiêu chuẩn chất lượng, dược liệu nhằm đảm bảo:
- Sự thống nhất trong rà soát hồ sơ, cách tiếp nhận và công bố tiêu chuẩn chất lượng dược liệu.
- Các bước cần thiết để tiếp nhận, rà soát hồ sơ và công bố tiêu chất lượng dược liệu nhằm quản lý chất lượng dược liệu một cách đầy đủ, có hệ thống theo đúng các quy định hiện hành và thủ tục hành chính.
Việc rà soát hồ sơ đề nghị công bố tiêu chuẩn chất lượng dược liệu của cơ sở kinh doanh.
3. TRÁCH NHIỆM THỰC HIỆN
- Lãnh đạo Cục, Lãnh đạo Phòng Quản lý Dược cổ truyền và các đơn vị có trách nhiệm thực hiện, tuân thủ, thường xuyên kiểm tra, đôn đốc, tổ chức thực hiện theo đúng quy định tại quy trình này.
- Bộ phận kế toán có trách nhiệm thực hiện, phối hợp thực hiện và đảm bảo những quy định trong quy trình này được thực hiện và tuân thủ.
- Chuyên viên có liên quan của Phòng Quản lý Dược cổ truyền, bộ phận một cửa có trách nhiệm thực hiện và tuân thủ những quy định trong quy trình này.
- Luật Dược số 105/2016/QH13 ngày 06/4/2016.
- Thông tư số 38/2021/TT-BYT ngày 31/12/2021 của Bộ trưởng Bộ Y tế quy định về chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền.
- Thông tư số 01/2018/TT-BYT ngày 18/01/2018 của Bộ trưởng Bộ Y tế quy định về ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc.
- Cục Quản lý YDCT: Cục Quản lý Y, Dược cổ truyền.
- Phòng QLDCT: Phòng Quản lý Dược cổ truyền.
- BM: Biểu mẫu.
- Hồ sơ: hồ sơ đề nghị công bố tiêu chuẩn chất lượng dược liệu.
- VTC: Văn thư Cục Quản lý YDCT.
- BP 1 cửa : Bộ phận 1 cửa - Văn phòng Cục.
- Cơ sở: Cơ sở kinh doanh (nuôi trồng, thu hái, khai thác, sản xuất, xuất khẩu, nhập khẩu, bán buôn, bán lẻ) dược liệu.
- Bản tự công bố: Bản tự công bố tiêu chuẩn chất lượng dược liệu.
- TCCL: Tiêu chuẩn chất lượng.
6. NỘI DUNG QUY TRÌNH
6.1. Sơ đồ quy trình:
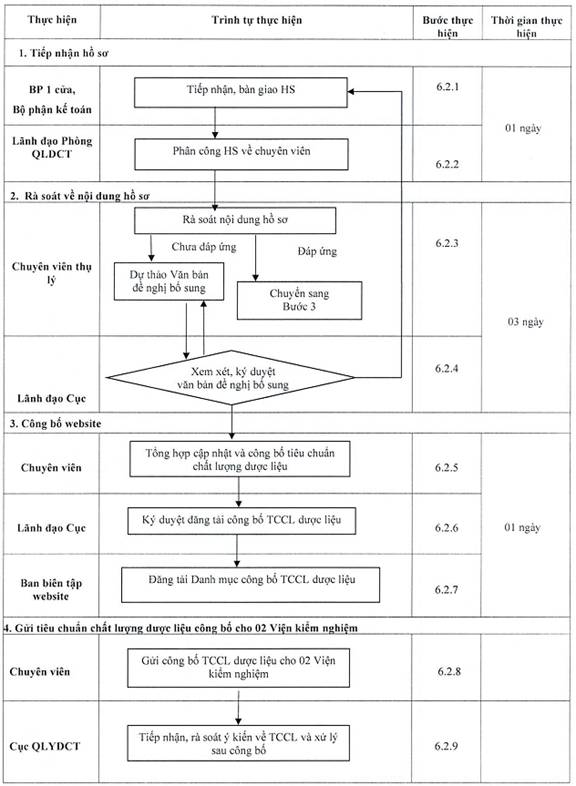
6.2. Mô tả quy trình:
Phần I: Bước 1. Tiếp nhận hồ sơ công bố tiêu chuẩn chất lượng dược liệu
Thời gian thực hiện: 01 ngày.
6.2.1. Tiếp nhận, bàn giao hồ sơ:
- Cơ sở thực hiện nộp hồ sơ công bố tiêu chuẩn chất lượng theo quy định tại Khoản 1 Điều 9 Thông tư 38/2021/TT-BYT.
- Bộ phận một cửa tiếp nhận, rà soát thành phần hồ sơ, gửi thông báo thu phí.
- Bộ phận kế toán thực hiện thu phí theo quy định.
- Sau khi hoàn tất thu phí và rà soát thành phần hồ sơ hợp lệ, bộ phận một cửa trả phiếu tiếp nhận theo biểu mẫu BM.CB.01 ban hành kèm theo SOP này; chuyển hồ sơ đến Phòng QLDCT và lập danh mục tổng hợp, báo cáo Lãnh đạo Cục theo biểu mẫu BM.CB.02.
6.2.2. Lãnh đạo Phòng QLDCT phân công hồ sơ đến chuyên viên thụ lý.
Phần II. Bước 2. Rà soát hồ sơ tự công bố
Thời gian thực hiện: 03 ngày.
6.2.3. Chuyên viên thụ lý rà soát thành phần hồ sơ công bố và rà soát tiêu chuẩn chất lượng của dược liệu đề nghị tự công bố. Kết quả rà soát được ghi vào Phiếu rà soát theo mẫu BM.CB.03 ban hành theo SOP này.
Trường hợp hồ sơ đáp ứng toàn bộ các nội dung tại Phiếu rà soát, chuyển sang Bước 3.
6.2.4. Trường hợp hồ sơ không đáp ứng một hoặc nhiều nội dung tại Phiếu rà soát, chuyên viên thụ lý dự thảo công văn đề nghị cơ sở bổ sung, chỉnh sửa, trình Lãnh đạo Phòng xem xét ký nháy và trình Lãnh đạo Cục ký ban hành.
Phần III. Bước 3. Công bố website
Thời gian thực hiện: 01 ngày.
6.2.5. Các hồ sơ đáp ứng các nội dung tại Phiếu rà soát, chuyên viên thụ lý xây dựng mã số công bố tiêu chuẩn chất lượng cho dược liệu, sau đó tổng hợp Danh mục các dược liệu công bố tiêu chuẩn chất lượng theo mẫu BM.CB.05 ban hành kèm theo SOP này, trình Lãnh đạo Phòng xem xét ký nháy và trình Lãnh đạo Cục ký phê duyệt.
6.2.6. Lãnh đạo Cục ký phê duyệt đăng tải công bố TCCL dược liệu.
6.2.7. Ban biên tập website Cục QLYDCT tiếp nhận Danh mục nêu trên để tiến hành đăng tải lên website của Cục QLYDCT theo quy trình đăng tải.
Phần IV. Bước 4. Gửi tiêu chuẩn chất lượng dược liệu công bố cho 02 Viện kiểm nghiệm
6.2.8. Chuyên viên thụ lý dự thảo công văn gửi TCCL kèm theo Danh mục các dược liệu dã được công bố tiêu chuẩn chất lượng trình Lãnh đạo Phòng QLDCT xem xét ký nháy và trình Lãnh đạo Cục ký ban hành.
Chuyên viên thụ lý gửi công văn, Danh mục dược liệu đã công bố tiêu chuẩn chất lượng và các bản tiêu chuẩn chất lượng của các dược liệu này kèm theo các tài liệu minh chứng khác (nếu có) gửi về 02 Viện Kiểm nghiệm: Viện Kiểm nghiệm thuốc Trung ương và Viện Kiểm nghiệm thuốc thành phố Hồ Chí Minh.
6.2.9. Trong quá trình kiểm soát chất lượng dược liệu, Viện Kiểm nghiệm thuốc Trung ương và Viện Kiểm nghiệm thuốc thành phố Hồ Chí Minh, các cơ sở kiểm nghiệm tỉnh, thành phố trực thuộc Trung ương có ý kiến phản hồi về các TCCL của các cơ sở đã được công bố và dựa trên kết quả từ các đợt kiểm tra, kiểm soát chất lượng của Bộ Y tế (Cục QLYDCT, Thanh tra Bộ), ý kiến của chuyên gia, Cục QLYDCT rà soát, xử lý theo quy trình SOP về xử lý sau công bố.
7. BIỂU MẪU
- BM.CB.01: Phiếu tiếp nhận công bố tiêu chuẩn chất lượng dược liệu.
- BM.CB.02: Danh mục hồ sơ tiếp nhận công bố tiêu chuẩn chất lượng dược liệu.
- BM.CB.03: Phiếu rà soát hồ sơ công bố tiêu chuẩn chất lượng dược liệu.
- BM.CB.04: Bản tự công bố tiêu chuẩn chất lượng dược liệu.
- BM.CB.05: Danh mục các dược liệu công bố tiêu chuẩn chất lượng.
| Ngày áp dụng: 29/12/2022 | Lần ban hành: 01 |
BM.CB.01: PHIẾU TIẾP NHẬN CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
| CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM | |
| Số: /PTN-CBDL | Hà Nội, ngày tháng năm |
PHIẾU TIẾP NHẬN
HỒ SƠ ĐỀ NGHỊ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
1. Tên dược liệu đề nghị công bố TCCL:
2. Tên cơ sở đề nghị công bố:
3. Địa chỉ cơ sở đề nghị công bố:
4. Số điện thoại liên hệ:
| STT | Thành phần hồ sơ | Số lượng |
| 1 | Bản tự công bố tiêu chuẩn chất lượng dược liệu theo Mẫu số 02 Phụ lục 1 ban hành kèm theo Thông tư số 38/2021/TT-BYT (bản Giấy và bản PDF). |
|
| 2 | Mẫu nhãn dự kiến của dược liệu. |
|
| 3 | Phiếu kiểm nghiệm dược liệu đạt theo tiêu chuẩn chất lượng đã công bố do cơ sở kiểm nghiệm thuốc, nguyên liệu làm thuốc đạt tiêu chuẩn Thực hành tốt phòng thí nghiệm thuốc (GLP) phát hành. |
|
| 4 | Giấy chứng nhận đạt tiêu chuẩn Thực hành tốt phòng thí nghiệm thuốc (GLP) của cơ sở phát hành Phiếu kiểm nghiệm. |
|
| 5 | Tài liệu chứng minh nguồn gốc, xuất xứ của dược liệu. |
|
| 6 | Quy trình sơ chế của dược liệu (nếu là dược liệu sơ chế) |
|
| 7 | Bảng so sánh tiêu chuẩn chất lượng của dược liệu công bố so với chuyên luận trong Dược điển (nếu có). |
|
| 8 | Tài liệu chứng minh để xây dựng tiêu chuẩn cơ sở (kết quả nghiên cứu khoa học, các kết quả thử nghiệm, đánh giá, phân tích) (nếu có). |
|
Ghi chú: Các tài liệu trong hồ sơ công bố phải được thể hiện bằng tiếng Việt; trường hợp có tài liệu bằng tiếng nước ngoài thì phải được dịch sang tiếng Việt hoặc tiếng Anh và được công chứng theo quy định. Tất cả các tài liệu phải còn hiệu lực khi công bố. Doanh nghiệp chịu trách nhiệm về tính pháp lý và nội dung của hồ sơ công bố.
Phiếu tiếp nhận này được lập thành 02 bản: 01 bản lưu tại Cục Quản lý Y, Dược cổ truyền và 01 bản gửi doanh nghiệp.
| NGƯỜI NỘP HỒ SƠ | NGƯỜI NHẬN HỒ SƠ |
BM.CB.02. DANH MỤC TIẾP NHẬN HỒ SƠ ĐỀ NGHỊ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
DANH MỤC TIẾP NHẬN HỒ SƠ ĐỀ NGHỊ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
| STT | Tên cơ sở đề nghị công bố | Tên dược liệu đề nghị công bố | Ngày tiếp nhận | Mã hồ sơ | Ghi chú |
| 1 |
|
|
|
|
|
| 2 |
|
|
|
|
|
| 3 |
|
|
|
|
|
|
| Hà Nội, ngày tháng năm |
| NGƯỜI BÀN GIAO | NGƯỜI TIẾP NHẬN |
BM.CB.03. PHIẾU RÀ SOÁT HỒ SƠ ĐỀ NGHỊ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
PHIẾU RÀ SOÁT HỒ SƠ ĐỀ NGHỊ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
I. Thông tin chung:
| Cơ sở đề nghị công bố: | Mã tiếp nhận: Ngày tiếp nhận: |
| Tên dược liệu đề nghị công bố: | Tiêu chuẩn chất lượng áp dụng: |
II. Kết quả xem xét
| STT | Nội dung rà soát | Căn cứ pháp lý rà soát | Kết quả rà soát | ||
| Đạt | Chưa đạt | Ghi chú | |||
| PHỤ LỤC I: RÀ SOÁT THÀNH PHẦN, TÍNH PHÁP LÝ CỦA HỒ SƠ | |||||
| 1. | Thông tin về tổ chức, cá nhân tự công bố tiêu chuẩn chất lượng dược liệu: | ||||
| 1.1. | Cơ sở đề nghị công bố thuộc đối tượng được công bố tiêu chuẩn chất lượng và các giấy tờ pháp lý của cơ sở. | Căn cứ các cơ sở được phép công bố TCCL dược liệu quy định tại Khoản 2 Điều 8 Thông tư số 38/2021/TT-BYT và Quy định về điều kiện kinh doanh dược hiện hành. |
|
|
|
| 2. | Dược liệu đề nghị công bố TCCL: | ||||
| 2.1. | Dược liệu thuộc đối tượng công bố TCCL | Căn cứ quy định tại Khoản 1 Điều 8 Thông tư số 38/2021/TT-BYT (ghi rõ có trong Dược điển hay không có trong Dược điển) |
|
|
|
| 3. | Bản công bố TCCL dược liệu: | ||||
| 3.1. | Đầy đủ các thông tin của bản công bố | Căn cứ Bản tự công bố TCCL dược liệu (Biểu mẫu số BM.CB.04) |
|
|
|
| 3.2. | Tên dược liệu đề nghị công bố | Căn cứ điểm a khoản 3 Điều 16 Thông tư số 01/2018/TT-BYT |
|
|
|
| 3.3. | Tên khoa học của dược liệu | Căn cứ điểm b khoản 3 Điều 16 Thông tư số 01/2018/TT-BYT |
|
|
|
| 3.4. | Nguồn gốc của dược liệu | Phù hợp với tài liệu chứng minh nguồn gốc xuất xứ của cơ sở tại hồ sơ đề nghị công bố |
|
|
|
| 4. | Rà soát mẫu nhãn: | ||||
| 4.1. | Có đủ các nội dung về nhãn dược liệu | Căn cứ Điều 7 Thông tư số 01/2018/TT- BYT |
|
|
|
| 5. | Phiếu kiểm nghiệm dược liệu: | ||||
| 5.1. | Giấy GLP của cơ sở kiểm nghiệm còn hiệu lực tại thời điểm phát hành phiếu kiểm nghiệm. | Hiệu lực của giấy và phạm vi kiểm nghiệm |
|
|
|
| 5.2. | Phiếu kiểm nghiệm có đầy đủ các chỉ tiêu chất lượng so với tiêu chuẩn chất lượng tự công bố. | Tiêu chuẩn chất lượng tự công bố của cơ sở |
|
|
|
| 6. | Tài liệu chứng minh nguồn gốc, xuất xứ của dược liệu: | ||||
| 6.1. | Đầy đủ tài liệu chứng minh nguồn gốc, xuất xứ của dược liệu | Căn cứ Điều 13 Thông tư số 38/2021/TT-BYT |
|
|
|
| PHỤ LỤC II: RÀ SOÁT TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU | |||||
| 7. | Dược liệu: | ||||
| 7.1. | Dược liệu có chuyên luận chất lượng trong Dược điển: |
|
|
| |
| 7.1.1 | Có đầy đủ các chỉ tiêu chất lượng. | Dược điển Việt Nam hoặc Dược điển các nước (tùy theo cơ sở áp dụng) |
|
|
|
| 7.1.2. | Có tối thiểu 01 chỉ tiêu có mức chất lượng cao hơn tiêu chuẩn Dược điển. | Dược điển Việt Nam hoặc Dược điển các nước (tùy theo cơ sở áp dụng) (ghi rõ chỉ tiêu có mức chất lượng cao hơn) |
|
|
|
| 7.2. | Dược liệu không có chuyên luận chất lượng trong Dược điển: |
|
|
| |
| 7.2.1 | Có kết quả nghiên cứu khoa học, các kết quả thử nghiệm, đánh giá, phân tích. | Kết quả nghiên cứu khoa học, các kết quả thử nghiệm, đánh giá, phân tích |
|
|
|
| 8. | Dược liệu sơ chế: | ||||
| 8.1. | Có các chỉ tiêu chất lượng của dược liệu trong Dược điển. | Dược điển Việt Nam hoặc Dược điển các nước (tùy theo cơ sở áp dụng) |
|
|
|
| 8.2. | Mức chỉ tiêu chất lượng: |
|
|
| |
| 8.2.1. | Trường hợp TCCS của dược liệu sơ chế có mức chất lượng bằng hoặc cao hơn mức chất lượng quy định trong Dược điển: phải có tối thiểu 01 chỉ tiêu có mức chất lượng cao hơn tiêu chuẩn Dược điển. | Dược điển Việt Nam hoặc Dược điển các nước (tùy theo cơ sở áp dụng) (ghi rõ chỉ tiêu có mức chất lượng cao hơn) |
|
|
|
| 8.2.2. | Trường hợp mức chất lượng thấp hơn mức chất lượng quy định trong Dược điển thì phải có kết quả nghiên cứu khoa học, các kết quả thử nghiệm, đánh giá, phân tích. | Kết quả nghiên cứu khoa học, các kết quả thử nghiệm, đánh giá, phân tích |
|
|
|
| II. Nội dung khác (nếu có)
| |||||
| Ý kiến đề xuất: | Ngày tháng năm 2022 |
| Chuyên viên
|
| Ý kiến của Phòng Quản lý DCT: | Ngày tháng năm 2022 |
| Lãnh đạo phòng
|
| Ý kiến của Lãnh đạo Cục | Ngày tháng năm 2022 |
| Lãnh đạo Cục
|
BM.CB.04. Bản tự công bố tiêu chuẩn chất lượng dược liệu
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập - Tự do - Hạnh phúc
---------------
BẢN TỰ CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG DƯỢC LIỆU
Số: ………………/Tên cơ sở công bố/Năm công bố
I. Thông tin về tổ chức, cá nhân tự công bố tiêu chuẩn chất lượng dược liệu
Tên cơ sở công bố: ....................................................................................................
Địa chỉ: .......................................................................................................................
Điện thoại: ………………………………… Fax: ................................................................
E-mail .........................................................................................................................
Mã số doanh nghiệp: ...................................................................................................
Số Giấy chứng nhận đủ điều kiện kinh doanh dược ……… ngày cấp ……… nơi cấp ......
II. Thông tin về sản phẩm
1. Tên dược liệu (tên khoa học): ...................................................................................
2. Nguồn gốc: .............................................................................................................
3. Quy cách đóng gói: .................................................................................................
4. Tên và địa chỉ cơ sở nuôi trồng, thu hái, khai thác (đối với dược liệu trong nước);......
5. Tên và địa chỉ cơ sở nhập khẩu (đối với dược liệu nhập khẩu): ..................................
III. Mẫu nhãn sản phẩm (đính kèm mẫu nhãn sản phẩm hoặc mẫu nhãn sản phẩm dự kiến)
IV. Tiêu chuẩn chất lượng công bố
(Tên cơ sở công bố) công bố dược liệu đạt tiêu chuẩn chất lượng do cơ sở xây dựng (Trường hợp tiêu chuẩn chất lượng công bố có chỉ tiêu chất lượng và mức chất lượng cao hơn so với Dược điển thì đính kèm bảng so sánh)
Đính kèm (Số: …………….).
Chúng tôi xin cam kết thực hiện đầy đủ các quy định của pháp luật về dược và hoàn toàn chịu trách nhiệm về tính pháp lý của hồ sơ công bố tiêu chuẩn chất lượng dược liệu mà... (tên cơ sở công bố) đã công bố./.
|
| ……….., ngày .... tháng .... năm ….. |
BM.CB.05
DANH MỤC CÁC DƯỢC LIỆU CÔNG BỐ TIÊU CHUẨN CHẤT LƯỢNG THEO THÔNG TƯ SỐ 38/2021/TT-BYT NGÀY 31/12/2021
(Cập nhật tới ngày/tháng/năm)
| STT | Tên dược liệu công bố | Tên khoa học | Nguồn gốc (1) | Số công bố TCCL hoặc số do công ty công bố | Tiêu chuẩn chất lượng áp dụng | Tên cơ sở công bố | Địa chỉ cơ sở công bố | Ngày công bố |
| 01 | Ba kích (sơ chế) |
| Trung Quốc | CB.DL- 00001-22 | TCCS | Công ty ... | Hà Nội | 01/01/2022 |
| 02 | Ba kích | ... | Việt Nam | CB.DL- 00002-22 | TCCS | Công ty ... | Hà Nội | 01/01/2022 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Chú thích: (1) Tên quốc gia nuôi trồng, thu hái dược liệu.
- 1Quyết định 545/QĐ-QLD năm 2022 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 2Quyết định 583/QĐ-QLD năm 2022 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 3Quyết định 18/QĐ-QLD năm 2023 Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 4Quyết định 2428/QĐ-BKHCN năm 2022 công bố Tiêu chuẩn quốc gia đối với Lợn giống bản địa và Quy trình khảo nghiệm, kiểm định giống vật nuôi do Bộ trưởng Bộ Khoa học và Công nghệ ban hành
- 5Quyết định 397/QĐ-QLD năm 2023 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 6Quyết định 3878/QĐ-BTNMT năm 2023 công bố Hệ thống quản lý chất lượng phù hợp Tiêu chuẩn quốc gia TCVN ISO 9001:2015 do Bộ trưởng Bộ Tài nguyên và Môi trường ban hành
- 1Quyết định 19/2014/QĐ-TTg áp dụng Hệ thống quản lý chất lượng theo Tiêu chuẩn quốc gia TCVN ISO 9001:2008 vào hoạt động của cơ quan, tổ chức thuộc hệ thống hành chính nhà nước do Thủ tướng Chính phủ ban hành
- 2Luật Dược 2016
- 3Thông tư 01/2018/TT-BYT về quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc do Bộ trưởng Bộ Y tế ban hành
- 4Công văn 419/BKHCN-TĐC năm 2018 về lộ trình chuyển đổi áp dụng hệ thống quản lý chất lượng theo tiêu chuẩn quốc gia TCVN ISO 9001:2015 do Bộ Khoa học và Công nghệ ban hành
- 5Thông tư 38/2021/TT-BYT quy định về chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền do Bộ trưởng Bộ Y tế ban hành
- 6Quyết định 545/QĐ-QLD năm 2022 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 7Quyết định 583/QĐ-QLD năm 2022 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 8Quyết định 18/QĐ-QLD năm 2023 Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 9Quyết định 2428/QĐ-BKHCN năm 2022 công bố Tiêu chuẩn quốc gia đối với Lợn giống bản địa và Quy trình khảo nghiệm, kiểm định giống vật nuôi do Bộ trưởng Bộ Khoa học và Công nghệ ban hành
- 10Quyết định 397/QĐ-QLD năm 2023 về Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược
- 11Quyết định 3878/QĐ-BTNMT năm 2023 công bố Hệ thống quản lý chất lượng phù hợp Tiêu chuẩn quốc gia TCVN ISO 9001:2015 do Bộ trưởng Bộ Tài nguyên và Môi trường ban hành
Quyết định 369/QĐ-YDCT năm 2022 công bố Hệ thống quản lý chất lượng phù hợp tiêu chuẩn quốc gia TCVN ISO 9001:2015 do Cục trưởng Cục Quản lý Y, Dược cổ truyền ban hành
- Số hiệu: 369/QĐ-YDCT
- Loại văn bản: Quyết định
- Ngày ban hành: 29/12/2022
- Nơi ban hành: Cục Quản lý Y, Dược cổ truyền
- Người ký: Nguyễn Thế Thịnh
- Ngày công báo: Đang cập nhật
- Số công báo: Đang cập nhật
- Ngày hiệu lực: 29/12/2022
- Tình trạng hiệu lực: Kiểm tra

